Rezultate
Etapa I: Stabilirea parametrilor tehnici de proiectare a sistemului combinat HF-DOT
Principalul obiectiv al acestui proiect este de a dezvolta o tehnica inovativa de mare acuratete bazata pe Tomografie Optica de Difuzie (DOT) asistata de fluorescenta de inalta rezolutie (HF), capabila sa aduca o contributie semnificativa tehnicilor clinice de investigatie mamografice existente.
Studiile teoretice si experimentale care se vor desfasura in cadrul proiectului sunt orientate in principal spre construirea unui dispozitiv combinat HF-DOT, impreuna cu optimizarea cai optice comune, elaborarea unui soft de reconstructie inovativ si acordarea unei atentii deosebite testelor cinice, atat in vitro cat si in vivo.
In aceasta etapa s-au stabilit parametri tenici de proiectare a sistemului combinat HF- DOT.
Proiectarea subsistemului DOT
La realizarea modelului de laborator se va avea in vedere următoarele cerinţe generale: Abilitatea de a efectua măsurători în paralel a intensităţii luminii provenite de la surse spectrale cu lungimi de undă diferite într-o gamă dinamică de valori ce depăşeşte 10^9 în condiţiile utilizării unor capete de măsură cu geometrie variabilă adaptabile cerinţelor impuse de structurile tisulare investigate. Asigurarea unor sensibilităţi de detecţie sub 20pW putere echivalentă de zgomot în condiţiile unor timpi de mediere relativi reduşi. Generarea unui număr multiplu de puncte de iluminare şi achiziţia semnalelor de măsură în condiţiile utilizării unor multiplexoare optice ce asigură poziţionarea reproductibilă a fasciculelor laser de diferite lungimi de undă pe ţesut în 2 – 64 de puncte de măsură. 9 Proiectul utilizat la realizarea modelului de laborator a instalaţiei de tomografie optică de difuzie a urmărit în principal realizarea următoarelor criterii: raport cost performanţă optimizat versatilitate aplicativă şi de configurare a modulelor simpitatea de interconectare optică şi electrică a modulelor controlul prin soft a principalilor parametrii caracteristici (putere laser emisă, câştig în liniile de amplificare, sincronizarea poziţionării fasciculelor în optode şi a achiziţiei de semnal, etc.) Modelul de laborator se va baza pe combinarea unei tehnici cu diode laser şi detectori optici (emisie si detecţie), cu elemente de mecanică si optică de precizie, cu sisteme de poziţionare a fibrelor optice de măsură la periferia ţesutului investigat (pentru ajustarea contactului fibrelor la geometria neregulată a ţesutului), cu fibre optice (distribuţia luminii la/dinspre capul de măsură), şi cunoştinţe de chimie şi medicină, măsurări electrice şi achiziţii de date, prelucrări soft-ware pentru testarea sistemului şi reconstrucţia imaginii ţesuturilor investigate.
Schema subsistemului DOT, prezentată în figura, este structurată pe următoarele elemente: • Sursa de iluminare multispectrală cu două diode laser (λ1 şi λ2) asistată de sisteme electronice pentru controlul stabilităţii puterii şi frecvenţei emise de diodele şi două generatoare de semnale de modulaţie pentru codarea prin frecvenţa de modulaţie, a identităţii sperctrale a radiaţiei emise. • Sisteme optice de colimare pentru cuplarea radiaţiei emise de diodele laser la fibra sumatoare şi la fibrele optice din optoda de măsură, la sursa de iluminare şi respectiv sistemul de detecţie a semnalelor măsurate • Două multiplexoare optice pentru iluminarea şi respectiv măsurarea semnalelor optice transmise prin ţesut pe structura de n fibre optice a unei optode circulare cu distribuţie radială a fibrelor optice • Sistem electronic de comandă a multiplexoarelor optice • Ansamblu electronic pentru detecţia, amplificarea, decodarea şi prelucrarea semnalelor luminoase recepţionate prin fibrele receptoare • Unitate de calcul pentru controlul funcţionării sursei de iluminare laser, multiplexoarelor optice, sistemului de achiziţie de date şi reconstrucţia grafică a structurii ţesutului investigat în baza datelor specifice de difuzie a luminii achiziţionate.
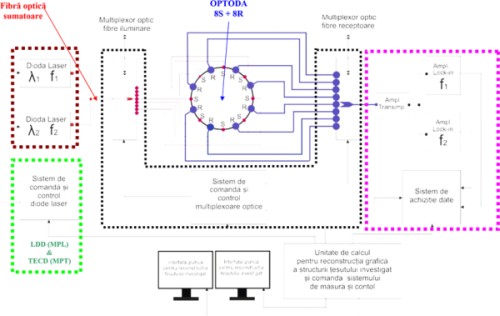
Sistemul de multiplexare - demultiplexare
Pentru subsistemul DOT am studiat posibilitatea folosirii unui multiplexor/demultiplexor care să nu folosească piese în miscare si care să poată comuta usor, fiabil si într-un timp cât mai scurt semnalul venit pe o fibră pe rând în opt fibre de iesire sau invers.
Acest lucru este posibil dacă folosim un comutator optic pentru fibre multimod cum ar fi cel produs de Sercalo, modelul SW1x8-62N. Caracteristicile sale sunt prezentate în tabelul de mai jos..

|
Unităti |
Minim |
Tipic |
Maxim |
Comutator |
|
|
|
|
Domeniul de lungimi de undă |
nm |
700 |
|
1700 |
Pierderile prin insertie 1 |
dB |
|
0,5 |
1,6 |
Diafonie |
dB |
|
55 |
45 |
Reflexie inversă |
dB |
|
45 |
35 |
Pierderi dependente de polarizare |
dB |
|
0,07 |
0,20 |
Timp de comutatie |
ms |
|
2 |
20 |
Tensiune de comutatie |
V |
|
|
5 |
Pigtail de fibră |
µm |
|
62,5/125/900 |
|
Durabilitate |
cicluri |
|
Nu se uzează |
|
Capsulă |
|
|
|
|
Consum |
mW |
|
40 |
|
Temperatura de operare |
°C |
0 |
|
70 |
Temperatura de stocare |
°C |
-40 |
|
85 |
Dimensiuni |
mm |
|
76 x 93 x 9,5 |
|
Proiectarea subsistemului Hiperspectral
Subsistemul Hiperspectral are ca element principal o cameră hiperspectrală, formată din obiectivul 1, spectrograful 2, camera video 3 si placa de bază 4. Camera hiperspectrală este fixată de stâlpul 7 prin intermediul suportului 5 si a clemei 6. Stâlpul 7 se fixează de masa de experiment prin intermediul bazei pentru stâlp 8.
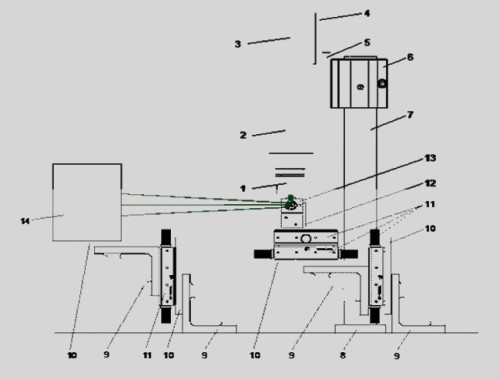
Deoarece camera hiperspectrală „vede” doar o fantă din câmpul obiect este necesar să se adauge un sistem de baleiaj, pentru a se obtine un câmp obiect de 28 x 28 mm. Pentru aceasta se foloseste un sistem galvanometric 13 cu o oglindă rotitoare, amplasat pe un suport reglabil pe trei axe, alcătuit din doi coltari 9, două suporturi măsută 10, trei măsute de translatie 11 si un suport galvanometru 12.
Recipientul cu proba 14, acelasi care a fost folosit si cu subsistemul DOT, este asezat pe un suport reglabil pe verticală, alcătuit din doi coltari 9, două suporturi măsută 10, si o măsută de translatie 11.
Camera hiperspectrală aleasă a fost camera SPECIM modelul PS-FW-11-V10-OEM . Ea este alcătuită din obiectivul Xenoplan 1.4/17, spectrograful Specim V10 si camera Kappa PS/DX4-285FW.
Caracteristicile camerei PS-FW-11-V10-OEM sunt prezentate în Tabelul 2.
Caracteristicile camerei SPECIM PS-FW-11-V10-OEM
PROPRIETĂI OPTICE |
|
Domeniul spectral |
400-1000 nm |
Rezolutia (spatială x spectrală) |
1392 x 1040 (990 linii active) |
Spectrograful |
ImSpector V10 |
Rezolutia spectrală |
6,8 nm (fantă de 30 μm) |
Esantionare spectrală |
0,63 – 5,0 nm/pixel |
Rezolutia spatială |
diametrul spotului RMS < 80 μm |
Aberatii |
distorsiunea de-a lungul axei spectrale < 45 μm distorsiunea de-a lungul axei spatiale < 40 μm |
Apertura numerică |
F/2.8 |
Lătimea fantei |
30 μm |
Lungimea efectivă a fantei |
8,98 mm |
Eficienta totală (tipică) |
> 50%, independent de polarizare |
Lumină parazită |
< 0.5% (lampă halogen, filtru trece-jos 590 nm) |
CARACTERISTICI ELECTRICE |
|
Senzor |
CCD Interlinie |
Interfată |
FireWire |
Iesire cameră |
Digital 12 biti |
Viteză de cadre (complet/ binning) |
11 Hz / 62 Hz (1 x 8 binning) |
Dimensiune pixel |
6,45 μm x 6,45 μm |
Controlul camerei |
FireWire |
Domeniul timpului de expunere |
1 μm - 120 s |
Consum |
< 5 W |
Tensiune de alimentare |
12 V |
CARACTERISTICI CLIMATICE |
|
Depozitare |
-20 la 50 °C |
Functionare |
5 la 40 °C fără condensare |
CARACTERISTICI MECANICE |
|
Dimensiuni (lungime x lătime x înăltime) |
220 x 60 x 70 mm |
Masă |
1,8 kg |
Corp |
Al anodizat cu găuri filetate de montaj |
Montura obiectivului |
C-Mount standard |
Interfata Labview
Datorita constructiei cu dezvoltare secventiala, proiectate pana in prezent, a fost necesara proiectarea separata a software-ului de control si achizitie date pe cele doua brate, HF si DOT. Astfel un program va asigura interfatarea cu comanda fotodiodelor, a amplificatorului lock-in si a multiplexorului din bratul DOT, iar cel de-al doilea program va include comanda galvanoscannerului, a camerei CCD, precum si rezultatul achizitiei imagistice din bratul HF.
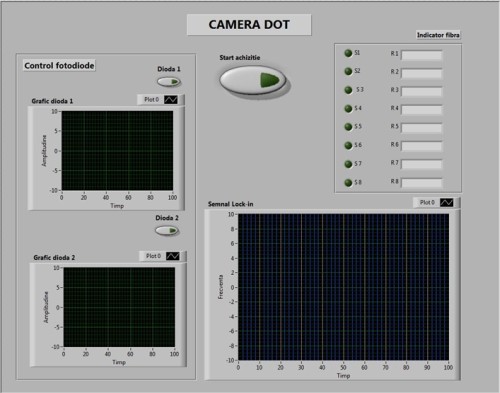
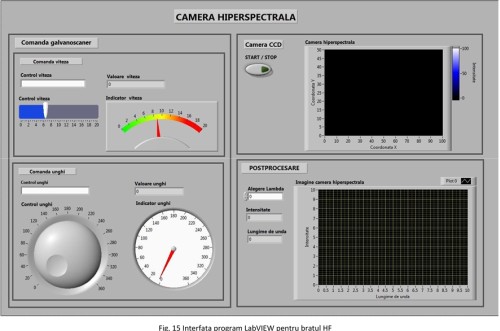
Aspecte Bio-Medicale
Tomografia Optica de Difuzie (DOT) foloseste natura selectiva a absorbtiei radiatiei luminoase. Absorbtia în tesut se datoreaza cromoforilor naturali ca pigmentul hem al hemoglobinei, mioglobina si bilirubina, pigmentii citocromi ai lantului respirator din mitocondrii, pigmentul melanin. In vizibil si infrarosu apropiat absorbtia este cauzata de cromofori specifici ca hemoglobina sau melanina.
Masuratorile multi spectrale ale fluctuatilor locale in stadiul de oxigenare al hemoglobinei (Hb) asigura explorarea dinamicilor spatio-temporale ale reactivitatii vasculare si gradul de oxigenare al HB, care are o importanta fundamentala in detectia tumorilor si raspunsul acestora la terapie. Din analiza datelor unor cancere precum melanomul malign sau angiosarcomul se poate abserva heterogeinitatea culorii (aparitia unor culori variate negru, maro, roşu, alb) indicand variatii in gradul de vascularizatie a tumorii.
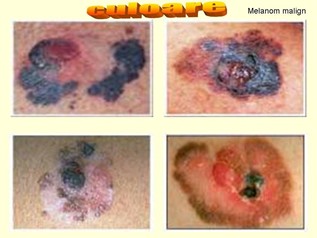
Melanomul malign cutanat este neoplazia cea mai severa a pielii; apare prin transformarea maligna a melanocitelor, celule de origine neuroectodermica ce sintetizeaza pigmentul melanina. Exista patru tipuri histologice, melanomul malign superficial fiind cel mai frecvent tip histologic de melanom malign (70%). Apare mai frecvent la femei, ca macule pigmentate, de culori variate (negru, maro, roşu, alb), cu margini neregulate, localizate in special pe fata posterioara a trunchiului. Grosimea tumorii (fost indice Breslow) se apreciază, tradiţional, cu micrometrul ocular în milimetri: Grupa I < 1 mm, Grupa II 1 – 2 mm, Grupa III 2 – 4 mm, Grupa IV > 4 mm.
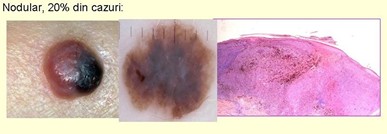
Un alt tip histologic mai frecvent de melanom malign (10-20%) este melanomul malign nodular. Leziunile, mai frecvente la barbati, sunt de culoare albastru inchis cu margine distincta şi cu o forma relativ simetrica si o creştere rapida.
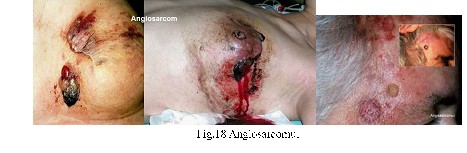
Angiosarcoame sunt tumorile maligne (cancere) care apar din celulele care sunt în mod normal utilizate pentru a face peretii vaselor de sange sau a vaselor limfatice. Angiosarcoamele pot apărea în orice organ al corpului, dar sunt mai frecvent găsite în piele si tesut moale. Ele pot fi de asemenea, în ficat, sân, splina, os sau inima. Semnele si simptomele angiosarcoamelor diferă în functie de localizarea tumorii. De multe ori simptome bolii nu sunt evidente până când tumora este destul de avansată.
Organului afectat |
Caracteristici |
Piele |
Prezenta unei vânătai, a unui nodul negru-albastru, sau a ulceratiilor nevindecate Leziunile pot sângera si pot fi dureroase |
San |
Extinderea rapida a masei palpabile fără sensibilitate De multe ori nu există nici o durere Tumorile de multe ori cresc adânc în tesutul mamar si provoaca mărirea sânilor difuz cu decolorarea pielii asociata cu albastrirea |
Mediile biologice sunt medii cu turbiditate, de aceea prezinta simultan absorbtiei si imprastiere, proprietatile de absorbtie ale tesutului fiind legate de biochimia tesutului, iar proprietatile de împrastiere de morfologia tesutului. Parametrii care caracterizeaza cele doua proprietati sunt coeficientul de absorbtie µ a [cm -1] si coeficientul de împrastiere µ s [cm -1]. Absorbtia si împrastierea luminii determina distributia sa spatiala în tesutul iradiat. Pentru diagnosticare, radiatia ce provine din tesut (adica reflectata difuz din tesut sau transmisa prin tesut) poate fi masurata pentru a proba starea metabolica, fiziologica sau structurala a tesutului.
Spectroscopia de fluorescenta este utilizata in mod intensiv de mult timp de catre medici si biologi folosind probele fluorescente. Spectroscopia de fluorescenta poate utiliza cromofori fluorescenti intrinseci prezenti in sistemele biologice, cum ar fi proteinele, acizii nucleici, si moleculele lipidice tisulare, pentru caracterizarea starii fiziologice a sistemelor normale sau anormale.
Glanda mamara prezinta o structura de tip stratificat format dint: invelis cutanat, stratul celular adipos premamar, corpul mamelei si stratul celular adipos retromamar.
Pielea este fina, mobila, cu putini foliculi pilosi si sebacei.
Tesutul celulo-adipos inconjoara glanda mamara in totalitate, mai putin areola mamara. Are o dispunere in doua straturi, premamar si retromamar.
Corpul mamar este alcatuit din doua elemente: parenchim si stroma.
Parenchimul glandei sau glanda mamara se compune dintr-un numar variabil (10-20, mai rar pana la 25) de glande elementare sau lobi. Lobii sunt separati intre ei prin tesut conjunctiv dens, in care se gaseste depozitata o mare cantitate de tesut adipos. La randul lor, lobii sunt subdivizati prin fine septuri conjunctive in lobuli. Fiecare lob e constituit dintr-o singura glanda tubulo-acinoasa (tubulo-alveolara) de tip apocrin formata dintr-un sistem canalicular foarte ramificat.
Stroma corpului mamar e de natura conjunctiva adipoasa si, la femeia negestanta, ea e intotdeauna mai abundenta decat sistemul canalicular (parenchimul), pe care il inconjoara din toate partile (lobi, lobuli). Intreg sistemul canalicular al unui lob e tributar unui canal colector principal, ductul lactifer sau canal galactofor. Stroma este strabatuta de numeroase vase sanguine si limfatice, nervi, precum si o bogata retea capilara. Distingem doua tipuri de stroma. In jurul ductelor mari si mijlocii se gaseste o stroma densa formata din fascicule de fibre conjunctive, e stroma interlobara si interlobulara. In jurul canaliculelor mici, stroma este reprezentata de tesut conjunctiv lax, mucoid si celular.
Dintre tumorile sanului, cea mai mare incidenta o are carcinomul invaziv ductal (75%) si carcinomul invaziv lobular (10%).
Fluorescenta, absorbtia si împrastierea luminii ofera informatii valoroase privind diferitele procesele fizice, chimice si biologice implicate, iar în unele cazuri metodele bazate pe aceste efecte sunt neinvazive. Utilizarea fluorescentei intrinseci devine din ce in ce mai des utilizata, putand caracteriza starea fiziologica a tesuturilor anormale în comparatie cu cele normale. Diferentele între spectrele de fluorescenta ale tumorilor canceroase si ale tesuturilor normale sunt atribuite transformarii mediului local ce înconjoara fluoroforii.
Analizele vor fi facute pe suprafete mari care includ atat tesut normal cat si tesut patogen. Aceste suprafete trebuie caroiate in suprafete mai mici care sa cuprinda atat zonele normale cat si cele patologice, eventual 4 zone care sa permita analiza leziunii compusa din diferite forme de manifestare a acesteia (variatii de culoare, de vascularizatie, hemoragii, etc) care sa defineasca suficient si necesar un fragment din leziune. Se vor analiza mai multe persoane si pe mai multe segmente, acelasi tip de leziune, scopul fiind acela de a gasi paternul de manifestare a leziunii in absorbtie si difuziune a luminii laser aplicate, pana la acest moment neexistand o semiologie oncologica in absorbtie si difuziune laser. Descoperirea unor substante (cromofori) caracteristice fiecarei leziuni, se face in etapa a doua cand leziunile vor fi analizate din punct de vedere al diferitelor metode spectroscopice (RMN, spectroscopie Raman, IR).
Modelarea Fantomelor
Pentru dezvoltarea tehnicii tomografice sunt necesare fantome cu proprietăţi fizice şi geometrice similare structurilor biologice investigate. Utilizarea fantomelor este esenţială în dezvoltarea algoritmilor de reconstrucţie grafică şi evaluarea performanţelor sistemului.
Coeficienţii de absorbţie şi împrăştiere reprezintă probabilitatea ca un foton sa fie absorbit sau împrăştiat la parcurgerea unei distanţe unitare în mediul investigat şi pot diferii cu ordine de mărime în funcţie de tipul de ţesut şi lungimea de undă a radiaţiei luminoase utilizate.
Mediul cel mai frecvent utilizat pentru realizarea fantomelor este intralipidul substanţă nutritivă administrată frecvent intravenos în unităţile medicale, ce reprezintă o emulsie în apă de fosfolipide. Proprietăţile optice ale intralipid-ului caracterizate în lucrările asigură la o concentraţie de 1% un mediu cu un coeficient de împrăştiere de aproximativ 1 mm-1 pentru radiaţii liminoase situate în infraroşu apropiat.
Deşi simplu de realizat, fantomele fluide necesită bariere din medii solide în care să fie inclus fluidul ce sunt caracterizate de proprietăţi optice diferite mediului fluid, iar stabilitatea în timp a acestora este redusă datorită instabilităţii fluidelor pentru perioade mai lungi de timp.
Fantomele lichide care pot fi folosite pentru masuratorile noastre sunt in principal:
- soluţii apoase injectabile de clorură de natriu (0,9%)
- soluţii diluate de intralipid (Lipofundin) în concentraţii de 1%, 2% şi 20% o soluţii diluate de hemoglobină animală
Alte fantome lichide pot fi obtinute, prin modificarea solutiilor mai sus mentionate cu aditivi, de genul cerneala, sau prin combinarea lor, in vederea obtinerii a diversi coeficienti optici care sa fiteze cat mai bine coeficientii reali a mai multor tipuri de tesuturi.
Pentru testarea algoritmilor de reconstrucţie şi a sensibilităţii tomografului optic de difuzie în fantomele menţionate cu structură omogenă se pot introduce si neomogenităţi controlate, sub forma de corpuri geometrice opace sau de volume cu propietăţi de absorbţie şi împrăştiere diferite de masa fantomei (de exemplu, tuburi cu soluţie de hemoglobină animală).
Dezavantajele privind instabilitatea solutiilor si complexitatea calculului de reconstructie, in cazul in care trebuie considerate si bariera solida, pot fi eliminate prin utilizarea de fantome solide.
Pentru realizarea acestor fantome se utilizează mase plastice cu proprietăţi semnificative de difuzie: cauciuc RTV, pigmenţi în mase de ceară, coloranţi, hemoglobină şi intralipid în gelatină, pulberi şi particule de oxid de aluminiu în mase siliconice, vopsele şi particule de dioxid de titan incluse în răşini epoxidice si răşini poliesterice.
Fantomele utilizate în calibrarea sistemelor tomografice sunt de cele mai multe ori cerute în geometrii similare tesuturilor investigate, ce prezintă o largă diversitate. Aceste fantome sunt în general proiectate si în raport cu dimensiunile şi specificul capului de măsură folosit în sistemul tomografic.
Geometriile diverse ale structurilor tisulare pot fi reproduse fidel şi stabil pentru perioade relativ lungi de timp (luni de zile) de fantomele solide.
Principalele materiale utilizate la realizarea fantomelor solide sunt siliconul, ceara, şi alcoolul polivinilic. Alcoolul polivinilic în amestec cu boraxul, devine semivâscos, sub forma unei mase noroioase, clară optic şi uşor configurabilă la valori predefinite de împrăştiere şi absorbţie, prin adăugarea în amestec de particule difuzante şi coloranţi.
Masa vâscoasă este închisă într-un înveliş flexibil de latex transparent în infraroşu apropiat, ce reproduce cât mai fidel structurile tisulare simulate.
Concluzii
In prezent, o serie de tehnici imagistice sunt folosite pentru detectia si monitorizarea tumorilor. In cazul tumorilor mamare, tehnicile principale sunt radiografia cu raze X, mamografia si RMN-ul. Rata lor de certitudine nu este atat de mare pe cat se doreste (rezultate fals pozitive sau fals negative), iar costurile ridicate restrictioneaza intrebuintarea acestora, si de cele mai multe ori este necesara biopsia in vederea stabilirii clare a tipului de tumoare. Pacientele se plang deja destul de mult de disconfortul mamografiei, astfel ca biopsia dubleaza stresul lor prin prisma naturii invazive si a timpului de asteptare pana la rezultatele finale.
Noi am propus un dispozitiv nou de imagistica, pe baza capacitatilor tehnicii DOT imbunatatite cu caracteristicile hiperspectrale ale fluorescentei intrinseci tisulare. DOT a fost deja folosit in monitorizarea activitatii cerebrale la noi nascuti, datorita caracterului noninvaziv, in timp ce fluorescenta se bazeaza strict pe semnalul receptionat de la fluorescenta intrinseca din corp, fara a fi nevoie de alte substante de contrast. Solutia abordata in proiectul nostru, de a combina tehnicile imagistice HF si DOT intr-un singur dispozitiv, este in topul metodelor imagistice de astăzi, consortiul nostru venind sa deschida o nouă cale în cercetarea si implementarea de instrumente de diagnostic inovatoare în practica clinică româneasca.
Atractivitatea sistemului de tomografie propus nu este data numai de caracterul neionizant al radiatiei folosite in acest dispozitiv si de costul redus al acestei tehnici de investigare, ci in principal de abilitatea de evidentiere a naturii patologice a leziunilor investigate, cu alte cuvinte, abilitatea de a distinge intre leziunile benigne si maligne, cu o rata de incertitudine de 8-10%, de doua ori mai mare decat tehnica curenta de mamografie cu raze X.
Drept urmare obiectivele de proiectare subsistemelelor DOT si Hiperspectral au fost indeplinite, urmand ca in etapa urmatoare sa se treaca la executarea acestora.
Diseminarea rezultatelor
* Prezentari orale/postere la conferinte nationale/internationale:
1.M.Patachia, S. Banita, C. Matei and D. C. Dumitras, „Multimodality Optical Imaging System for Intraoperative Detection of Tumor Positive Margins”, 3rd International Conference on Health Science and Biomedical Systems (HSBS14), Florence, Italy, November 22-24, 2014 (Oral).
3. M. Tautan, , I.S. Dontu,, D. Savastru, , M. A. Calin, S. Miclos, M.I. Rusu, C. Matei, M. Patachia, „APPLICATION OF HYPERSPECTRAL IMAGING METHOD FOR SKIN LESIONS DIAGNOSIS”, The Third International Conference on Analytical and Nonanalytical Methods for Biomedical and Environmental Sciences “IC - ANMBES 2014” June 13th - 15th, 2014, Brasov, Romania (Poster).
* Articole Publicate:
1. M. Paţachia, C. Popa, Ş Băniţă, and D. C. Dumitraş, “Acquisition and electrical signal processing in an experimental CW-Diffuse Optical Tomography system”, Rom. Rep. Phys., Vol. 67 (2014).
2. M. Paţachia, C. Popa, Ş Băniţă, and D. C. Dumitraş, „Continuous wave diffuse optical tomography system tested on phantoms and animal tissues”, Rom. Rep. Phys.,Vol. 67, No. 2, pp 412-422, 2015.



